首页
实验室张照亮团队与中科大龚为民团队合作在茶氨酸合成关键酶进化机制及其工程化生产方面取得重要进展
文章来源:
点击数:
更新日期::2023-12-10
茶氨酸是茶树中特异且含量最为丰富的非蛋白氨基酸,赋予茶叶鲜爽味,且具有镇静安神、提升睡眠质量、提高学习和认知能力等健康功效,其合成前体是乙胺和谷氨酸。茶树能特异性地合成乙胺是去区别于其它生物大量合成茶氨酸的代谢基础。催化乙胺合成的丙氨酸脱羧酶(CsAlaDC)是由丝氨酸脱羧酶(SerDC)进化而来,在此过程中,CsAlaDC底物由丝氨酸变为丙氨酸,但其催化活性与SerDC相比显著降低,但背后的进化机制尚不清楚。
近日,实验室张照亮教授团队与中国科学技术大学龚为民教授团队合作在国际著名生物学综合期刊《eLife》上在线发表了题为“Structure and evolution of Alanine/Serine Decarboxylases and the engineering of theanine production”的研究论文,揭示了CsAlaDC底物特异性和酶活性进化的结构特征,获得了高活性的CsAlaDC,实现了体外高效合成茶氨酸,为工业化合成茶氨酸提供了新方案。

本研究解析了CsAlaDC和AtSerDC的蛋白结构,表征了底物结合口袋的结构特征。基于此,通过对CsAlaDC和AtSerDC的底物结合口袋中的氨基酸残基叠加,发现CsAlaDC第106位的Phe (F)在AtSerDC对应位置上是酪氨酸Tyr (Y),而口袋中其余氨基酸残基完全相同(图1A)。通过分析400多个有胚植物中的SerDC蛋白序列,发现CsAlaDC 106Y或AtSerDC 110F位于一个保守的功能域中,在绝大数同源蛋白中该功能域的前三个氨基酸是YPY,而CsAlaDC的这三个氨基为YPF(图1B-D)。进而,通过点突变及体内、体外酶活等实验证明了CsAlaDC中106位的Phe决定其结合丙氨酸的底物特异性。
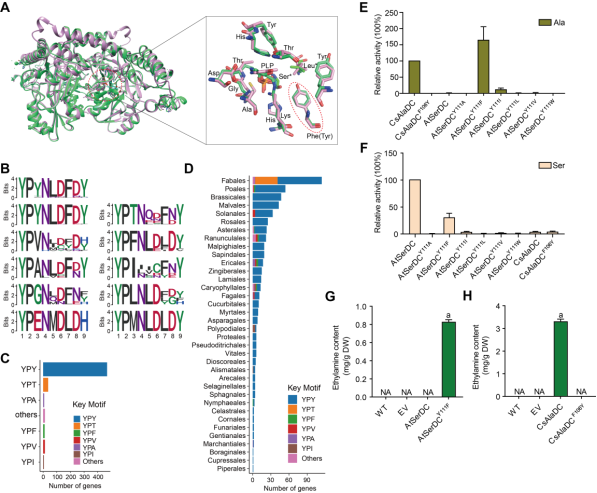
图1 决定CsAlaDC底物特异性关键氨基酸残基的鉴定
CsAlaDC或AtSerDC的蛋白结构为同源二聚体(图1A)。分析发现其同源二聚体结合界面上氨基酸对它们的催化活性至关重要。基于二聚体结合界面上氨基酸的突变筛选,发现把CsAlaDC二聚体界面上110位的异亮氨酸(L)、114位的酪氨酸(P)分别突变为SerDC对应位置上的苯丙氨酸(F)、丙氨酸(A),分别使CsAlaDC的催化活性提高了2.1和1.59倍。而这两个氨基酸同时突变(CsAlaDCL110F/P114A)时,催化活性提高了2.3倍(图2A)。更为重要的是,将CsAlaDCL110F/P114A与来自枯草芽孢杆菌的茶氨酸合成酶GMAS混合时,在提供丙氨酸和谷氨酸的条件下,体外合成茶氨酸的能力提高了6.72倍(图2B)。
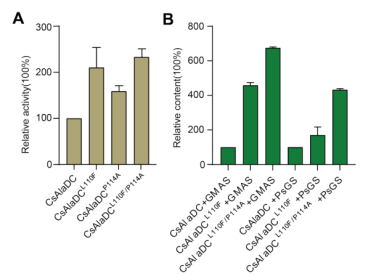
图2 决定CsAlaDC酶活性关键氨基酸残基的鉴定与体外高效合成茶氨酸
该研究揭示了茶树获得茶氨酸合成能力的序列进化和结构生物学基础,对高茶氨酸茶树品种的精准选育和茶氨酸的高效工业化合成有重要意义。实验室张照亮教授和中国科学技术大学龚为民教授为本论文共同通讯作者,中国科学技术大学王浩博士和重点实验室朱碧莹博士为共同第一作者,实验室宛晓春教授也参与了该研究。中国科学技术大学为论文第一通讯单位、安徽农业大学为第二通讯单位。该研究得到了科技部重点研发项目和国家自然科学基金项目的支持。

